| 应用 | 靶点发现 | 临床前开发 |
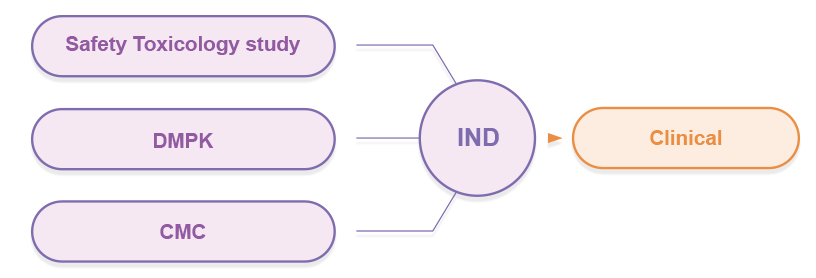
临床试验 申请 |
临床研究 | |||||
| 靶点筛选 靶点功能验证 | 动物体内药效/ 安全性药理毒理 | IIT | 临床 | ||||||
| QMS |
ISO9001
|
GMP-like
|
cGMP
|
||||||
- 丰富的经验:成功交付48+批次GMP sgRNA支持CGT企业中美或中欧临床申报
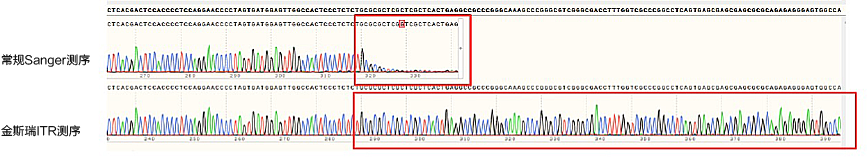
- 严格的质控:10+项定制化QC可选,高灵敏NGS检测sgRNA序列正确性,专利QC技术
- 定制化质量研究项目:为申报制定的质量研究项目,有机残留、超长截短序列分析、长期稳定性等
- IND申报支持:提供符合CDE申报要求的生产环境、文件记录、申报资料